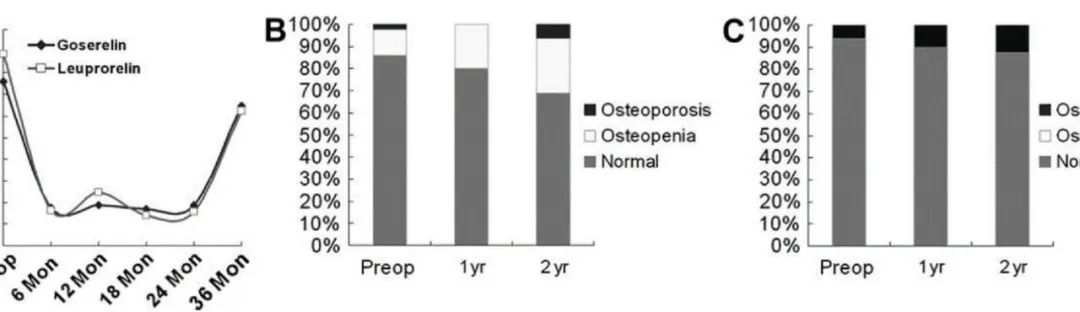
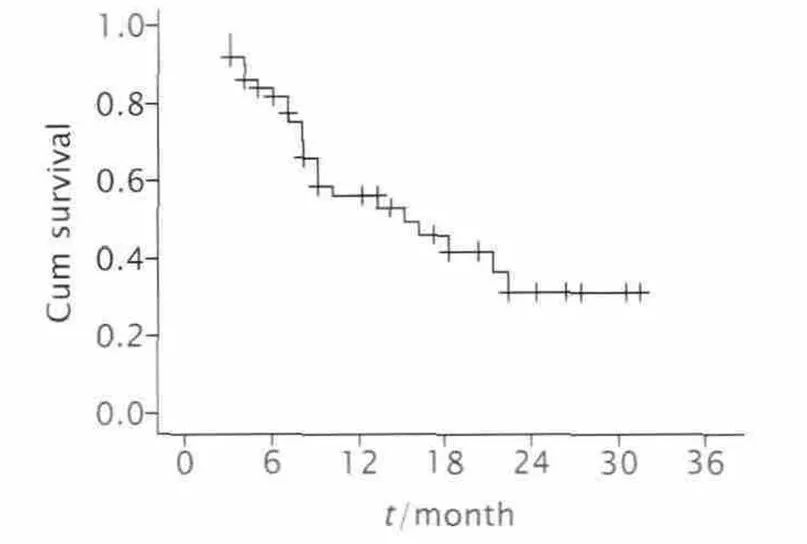
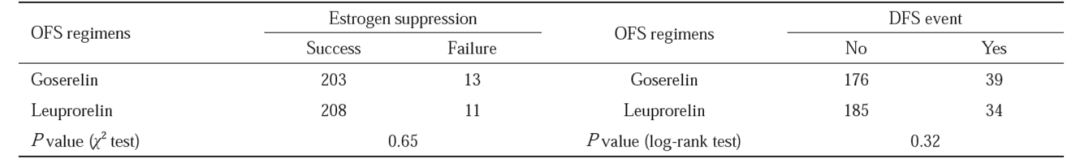
近年来,乳腺癌的发病率已经超越肺癌,成为全球范围内的第一大癌种 [1]。在中国,乳腺癌发病年轻化趋势较欧美国家更显著,后者年轻乳腺癌患者所占比例不到7%,而中国乳腺癌的年轻患者比例超过10%,中位诊断年龄为48~50岁,约有60%的患者在诊断时为绝经前状态 [2]。卵巢功能抑制 (Ovarian Function Suppression, OFS) 或称卵巢去势治疗,是绝经前激素受体阳性乳腺癌内分泌治疗的主要策略。国内外诊疗指南均推荐中高危早期绝经前激素受体阳性乳腺癌患者在辅助内分泌治疗期间联合GnRHa类药物 [3,4,5],作为此类患者内分泌治疗的基石,GnRHa的作用机制、药物疗效、以及预后等临床证据,本文将进行一一阐述。 天然的促性腺激素释放激素 (Gonadotropin-releasing hormone, GnRH) 是由人体下丘脑肽能神经元合成分泌的十肽激素,通过垂体门脉系统,脉冲式释放并刺激垂体前叶细胞合成卵泡刺激素 (FSH) 和黄体生成素 (LH);后两者分别在女性刺激卵巢分泌雌二醇和孕酮、在男性刺激睾丸生成睾酮,进而对人体生殖系统的各项生理功能产生调节作用。1971年,Andrew V. Schally 等最早从实验动物体内成功分离并合成出 GnRH 多肽化合物 [6]。在之后的研究发现,GnRH的第6位和第10位氨基酸起到非常关键的作用,通过替换GnRH的第6位和第10位氨基酸,可以延长药物的半衰期,增加它对蛋白分解酶的抵抗力以及细胞膜表面G蛋白偶联受体的GnRH的受体亲和性,大大提高对LH的释放活性。GnRH 激动剂或类似物 (GnRH agonist or analog, GnRHa) 通过竞争性结合垂体前叶的GnRH受体,长期使用后可导致垂体细胞GnRH受体的下调和脱敏,导致LH和FSH的分泌减少,从而达到抑制卵巢功能和降低雌激素分泌的目的,减缓雌激素受体 (Estrogen receptor, ER) 阳性乳腺癌细胞的生长 [7]。在人工合成的GnRHa类药物中,以亮丙瑞林、曲普瑞林和戈舍瑞林最为常见,其中亮丙瑞林的适应症则包括了乳腺癌、子宫内膜异位症、子宫肌瘤、前列腺癌和儿童中枢性性早熟等五大类疾病,在全球范围内具有应用人群广、历史长、疗效稳定、证据确切等特点。 OFS在乳腺癌治疗中作用的研究已经进行了数十年。早期研究发现 [8],通过手术、放疗等手段切除卵巢能明显降低乳腺癌的风险,改善早期乳腺癌患者的预后。由于OFS药物仅引起卵巢功能的可逆性改变,因此临床上多以药物作为卵巢去势的首选手段。既往研究发现 [9-10],与单独的OFS治疗 (ECOG 5188试验) 或单独的TAM治疗 (SOFT/TEXT试验和ASTRRA试验) 相比,OFS联合TAM (OFS+TAM) 治疗均能够显著改善患者的生存情况。SOFT/TEXT和STAGE两项临床试验结果显示,与OFS+TAM相比,OFS+AI在辅助治疗和新辅助治疗中均能够给绝经前激素受体阳性乳腺癌患者带来更好的获益。 多项研究证明,亮丙瑞林用于治疗绝经前HR阳性乳腺癌患者的短期雌激素抑制效果和长期无病生存率均有获益。2007年的TABLE研究 [11],纳入欧洲71家医疗中心,入组599例患者,中位随访5.8年,亮丙瑞林在总体生存率方面优于化疗方案 (81.0% vs. 71.9%, P=.005)。2009年在韩国一项纳入587 例接受GnRHa联合Tamoxifen/ target=_blank class=infotextkey>他莫昔芬治疗的绝经前乳腺癌患者的临床研究中,亮丙瑞林显示出良好的卵巢功能抑制作用,亮丙瑞林与戈舍瑞林的疗效和不良反应发生率无明显差异 [12] (图1. 雌激素的变化与不良反应)。 我国一项研究 [13] 纳入51例患者,均为绝经前复发或转移性乳腺癌,确诊为乳腺癌的中位年龄为45岁,结果显示51例患者的客观缓解率为21.6%(11/51),临床获益率为72.5%(37/51),中位无进展生存期为15.2个月(95% CI: 6.3-24.2个月)。单因素分析结果显示,雌激素受体和孕激素受体均为阳性、无病生存期≥2年患者以及未接受一线解救化疗患者的中位无进展生存期分别优于雌激素受体或孕激素受体为阳性(分别为21.3 和8.1个月,P=0.002)、无病生存期<2年(分别为21.3和8.1个月,P=0.005)以及接受一线解救化疗(分别为21.3和9.2个月,P=0.026)的患者。多因素分析结果显示,雌激素/孕激素状态是无进展生存期的独立预后因素 (图2. 51例绝经前复发或转移性乳腺癌患者接受亮丙瑞林微球联合芳香化酶抑制剂治疗的无进展生存曲线)。 另外一项研究 [14] 纳入435例接受OFS治疗的可手术乳腺癌患者,不同OFS药物如戈舍瑞林和亮丙瑞林的雌激素抑制作用基本一致(P>0.05)。内分泌治疗方案(HR = 0.49,P<0.05)、腋窝淋巴结状态(HR = 4.21,P<0.05)和肿瘤直径(HR = 2.00,P<0.05)均是患者DFS的独立预后因素;虽然雌激素抑制失败患者倾向预后较差(P = 0.10),但不同OFS药物对降低复发转移的疗效也一致。研究提示,年龄是乳腺癌患者采用OFS治疗后短期雌激素抑制失败的独立危险因素;内分泌药物、腋窝淋巴结状态以及肿瘤直径会影响ER阳性可手术乳腺癌患者的长期预后;无论是戈舍瑞林还是亮丙瑞林对患者降低雌激素水平和长期无病生存期差异无统计学意义 (图3. 不同GnRHa药物的短期效应和长期生存分析)。 在不良反应方面,国内研究者基于美国FAERS数据库分析 [15],收集了亮丙瑞林和戈舍瑞林不良反应信号,通过报告比值比 (ROR) 法和比例报告比值 (PRR) 法进行不良反应 (ADR) 信号挖掘,最终得到亮丙瑞林不良反应信号52个,戈舍瑞林不良反应信号100个,其中有17个信号为两者的重叠信号。将筛选出的ADR信号按累及器官/系统进行分类统计,亮丙瑞林共累及17个器官系统,戈舍瑞林共累及21个器官系统。其中,在戈舍瑞林共累及的神经紊乱、胃肠系统损害、心率及心律紊乱、听觉和前庭功能损害等4个器官系统中,未检测到亮丙瑞林的ADR信号,提示上述器官系统基础疾病患者,应谨慎选择戈舍瑞林作为药物治疗方案 (图4. 两种GnRHa药物不良反应信号的比较)。 在微球制剂制备工艺方面,各类GnRHa药物也有所区别,亮丙瑞林微球采用溶剂挥发法制备,而戈舍瑞林植入剂采用热熔挤出技术;与前者相比,后者制备中有高温过程,容易产生杂质,可能对药物活性成分的理化性质产生影响 [16]。这可能是导致两种药物临床疗效产生差异的影响因素之一。 结论: 亮丙瑞林治疗绝经前HR阳性乳腺癌患者的疗效肯定,是乳腺癌内分泌治疗的确切有效方案,可作为激素依赖型绝经前复发或转移性乳腺癌患者的一线治疗方案。 参考文献 1. Data source: GLOBOCAN 2020. http://gco.iarc.fr. Website of IARC (International Agency for Research on Cancer, WHO) 2. Fan L. Breast cancer in China. Lancet Oncol. 2014;15(7):e279-e289 3. Gradishar WJ. Breast Cancer. NCCN Clinical Practice Guidelines in Oncology. 2023;Version 4. March 23, 2023 4. 中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范 (2021年版).中国癌症杂志. 2021;31(10):954-1040 5. 江泽飞等.中国临床肿瘤学会 (CSCO) 乳腺癌诊疗指南 2023.人民卫生出版社. 2023年3月第1版 6. Huerta-Reyes M. Treatment of Breast Cancer with Gonadotropin-Releasing Hormone Analogs. Front Oncol. 2019;9:943 7. Fujino M. Synthetic analogs of luteinizing hormone releasing hormone (LH-RH) substituted in position 6 and 10. Biochem Biophys Res Commun. 1974;60(1):406-413 8. Lu YS. Ovarian Function Suppression with Luteinizing Hormone-Releasing Hormone Agonists for the Treatment of Hormone Receptor-Positive Early Breast Cancer in Premenopausal Women. Front Oncol. 2021;11:700722 9. Francis PA. Tailoring Adjuvant Endocrine Therapy for Premenopausal Breast Cancer. N Engl J Med. 2018;379(2):122-137 10. Kim HA. Adding Ovarian Suppression to Tamoxifen for Premenopausal Breast Cancer: A Randomized Phase III Trial. J Clin Oncol. 2020;38(5):434-443 11. Schmid P. Leuprorelin acetate every-3-months depot versus cyclophosphamide, methotrexate, and fluorouracil as adjuvant treatment in premenopausal patients with node-positive breast cancer: the TABLE study. J Clin Oncol. 2007;25(18):2509-2515 12. Kim HJ. Short term results from GnRH analogue use in pre-menopausal breast cancer in Korea. Eur J Surg Oncol. 2009;35(9):936-941 13. 梁旭. 亮丙瑞林微球药物性卵巢功能去势联合芳香化酶抑制剂治疗绝经前复发或转移性乳腺癌患者的临床研究. 肿瘤. 2014;34(10):941-945. 14. 刘燚铭. 卵巢功能抑制治疗雌激素受体阳性早期乳腺癌的短期效应和长期生存的影响因素分析. 中国癌症杂志. 2022;32(8):705-711 15. 陈乾. 基于美国FAERS数据库亮丙瑞林和戈舍瑞林不良反应信号检测. 医药导报. 2020;39(10):1366-1374 16. 李想. 长效微球制剂产业化研究进展.中国药学杂志. 2019;54(21):1729-1733